乳腺干细胞及再生医学
乳腺作为出生后发育的器官,在成体干细胞研究中具有得天独厚的优势。随着个体进入青春期,乳腺也会进入一个快速发育的阶段,在这一时期,乳腺干细胞的自我更新十分旺盛,从而构建形成完整的乳腺结构。乳腺的第二个快速发育阶段是在怀孕时,这一时期,乳腺干细胞会被重新活化,通过不断自我更新来满足孕期乳腺发育对多种细胞类型的需求。
乳腺是一个高度再生的器官,可以经历多个增殖、泌乳和复旧等周期,这些过程是通过乳腺干细胞来调控的。近10年来,乳腺干细胞在调控正常乳腺自我更新、上皮分化及其信号转导通路等方面的研究有了很大的进展,并且发现在乳腺的癌变中,调控生理性乳腺发育和稳态的信号转导通路异常起到重要的作用。
乳腺干细胞具有产生各类乳腺细胞的能力,其研究对于乳腺发育的认知、乳腺癌的治疗仪器乳腺器具的开发都具有重要意义。此外,伴随胎儿发育,胚胎期乳腺干细胞所经历的增殖、迁移、侵袭等过程是成体乳腺干细胞没有的,而这些经历与乳腺癌的发生过程非常相似。因此,针对乳腺干细胞的研究在医学上具有更重要的意义。
乳腺的基本结构
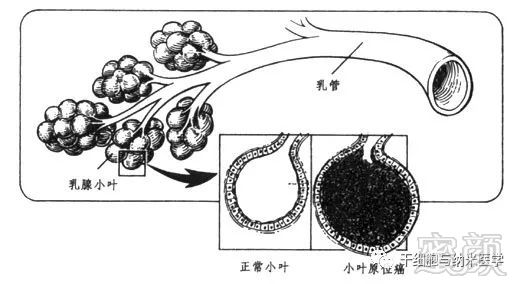
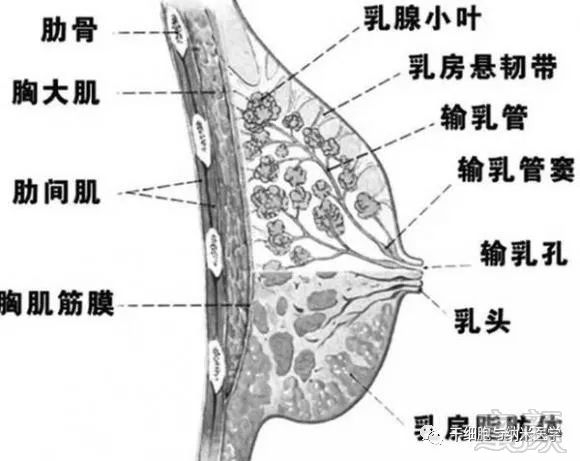
成人乳腺包括皮肤、皮下组织与乳腺组织三种结构。乳腺组织位于皮下浅筋膜的深浅两层间隙之中,由实质与间质组成。乳腺实质是由一系列分支而管径递减的管道系统构成,其中输乳管分出的腺叶导管系统构成腺叶。每个腺叶导管又在分出小叶导管,小叶导管再继续分出小叶外导管、小叶内导管、终端小导管与腺泡。
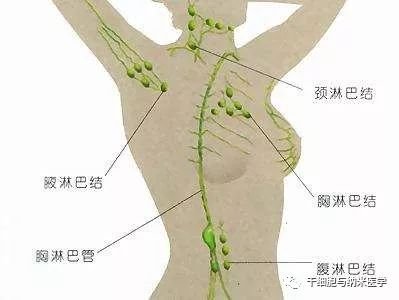
在女性乳房的组织内有极其丰富的淋巴管互相吻和成从,整个腺体、腺叶、腋小叶都被稠密而微细的淋巴网所包围。但小叶内无淋巴管。乳房的淋巴循环主要引流到腋窝淋巴结、内乳淋巴结、锁骨下/上淋巴结、腹壁淋巴管及两侧乳房皮下淋巴网的交通。其中蕞重要的是腋窝淋巴结和乳腺内侧淋巴结,它们是乳房淋巴引流的第壹站。乳房各个象限的淋巴液都可以向腋窝或内乳淋巴结引流,腋窝淋巴结收集约75%的乳房淋巴液,另外约25%流向乳腺内测淋巴结。因此,乳房外侧的肿瘤向腋窝淋巴结转移较多,肿瘤位于内侧时内乳淋巴结的转移率较高。
乳腺干细胞
妇女进入青春期乳腺充分发育后,在每一次月经周期以及妊娠、哺乳与断乳过程,乳腺会发生周期性增生或/和凋亡。在乳腺上皮中,有时可发现具有未分化形态的细胞,包括基底透明细胞和细胞角蛋白19阴性细胞。在乳腺导管发育过程中,位于终末导管终端芽(TEB)尖端的“帽细胞”属于干细胞。帽细胞具活跃的核分裂,其表型介于腔细胞和肌上皮之间,两者的标记如波形蛋白,SMA与黏蛋白呈明显低表达。它们如果迁移入TEB的腔细胞群中,发育成腔细胞;如果向侧面迁移至腔细胞与纤维基质之间,则变为肌上皮细胞。鉴于其分裂活性与不同的表型发展,有些学者因而设想,帽细胞是一种多潜能乳腺干细胞/祖细胞。但是,TEB只是一种过渡性结构,当导管延伸至脂肪垫后,TEB及其帽细胞即随之消失。成人乳腺的整个上皮群体均保持再生能力,因而帽细胞可能不是惟一的多能性乳腺上皮细胞。
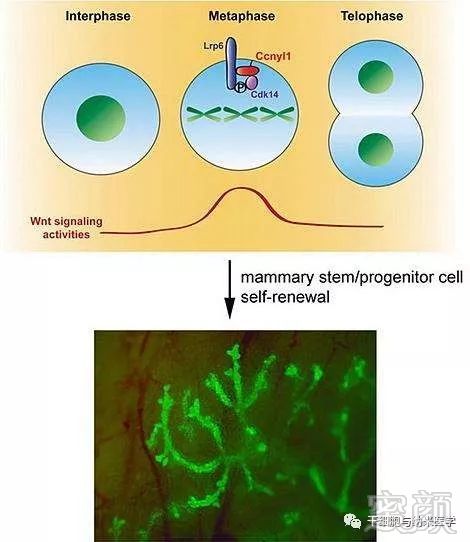
乳腺上皮干细胞具有长寿性、自我更新性、细胞分裂不对称性及克降性。
1. 长寿性:人乳腺上皮体外培养,均可传代50代以上。
2. 自我更新性:乳腺干细胞由于数量少、寿命长及子代祖细胞的扩增,使其自我更新的体外观察实验存在困难。在小鼠可用移植传代方法观察乳腺干细胞的自我更新。对人类乳腺干细胞自我更新能力的观察,乳腺干细胞的自我更新性与乳腺组织再生密切相关。
3. 细胞分裂不对称性:干细胞经不对称细胞分裂,产生了一个干细胞子代与另一个向系特异性细胞分化的子代。
4. 克隆性:单个乳腺干细胞经短期克隆培养。可以分别产生具有腔上皮、肌上皮分化与干/祖细胞样的克隆。
乳腺的再生医学
正常人体乳腺上皮增生或再生,至少影响因素之一是其体内雌激素和孕激素的水平。丰乳的某些药物或食品也不无与此类激素有关,此类药物对人类危害很大,可能诱发乳腺癌及多种生殖系统肿瘤和疾病。
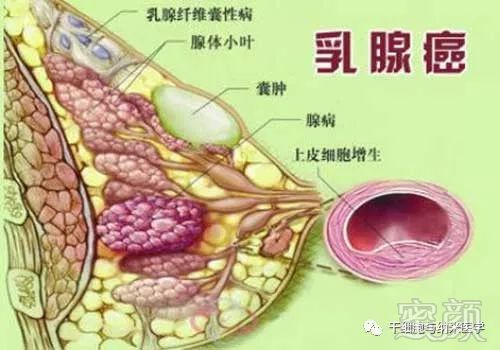
乳腺上皮细胞的损伤,可以是完全再生,即由损伤周围的同种细胞进行修复;也可以是不完全性再生,即由纤维结缔组织来修复,称为纤维性修复。乳腺上皮细胞再生可以是生理性再生,也可以是病理性再生。乳腺属于成人激素依赖性器官和组织,随着生理过程的变化,组织和细胞不断老化,乳腺上皮细胞可以发生凋亡,由新生的同种细胞不断补充,以保持原有细胞结构和功能,即生理性再生;也可以在各种病理状态下,组织和上皮细胞损伤后的再生,即病理性再生。乳腺上皮再生来自于具有自我更新和分化潜能的乳腺干/祖细胞,再生的结果可能从正常增生到不同程度的非典型性增生,甚至癌变,所以要引起临床注意。
乳腺干细胞在临床乳腺再生、乳腺组织工程和转化医学中起着重要的作用,具有广阔的临床应用前景。理论上,使用人体乳腺干细胞可以再生乳腺,可用于乳房切除术后的再造乳房手术或隆胸手术。
